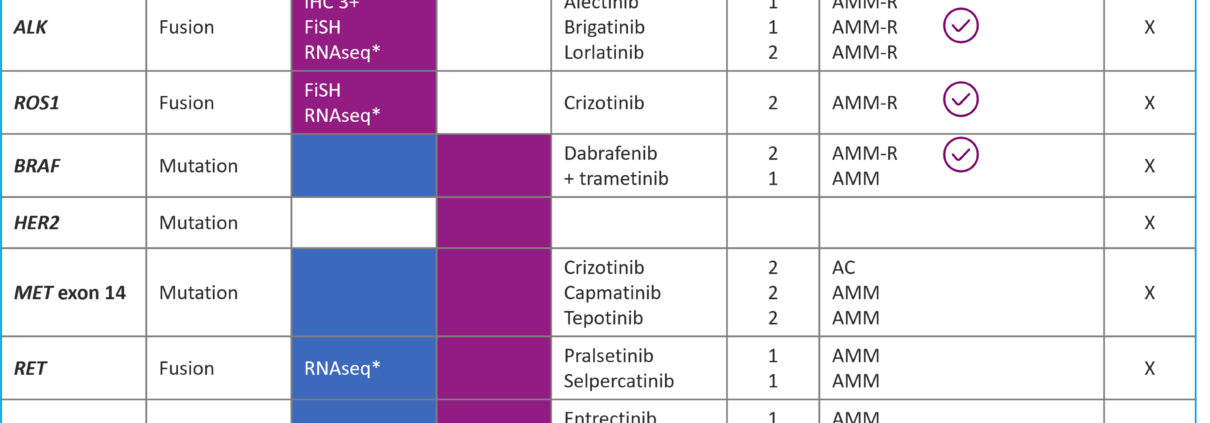
Thérapies ciblées dans les CBNPC métastatiques, quels accès en 2022 ?
La recherche d’addictions oncogéniques fait partie intégrante de la prise en charge des cancers bronchiques non à petites cellules (CBNPC) non épidermoïdes et des épidermoïdes du non-fumeur. Elle impacte la première ligne de traitement, premièrement en permettant l’accès à des thérapeutiques efficaces impactant directement la survie des patients, mais également en permettant d’éviter des traitements potentiellement inefficaces (ex : immunothérapie en monothérapie chez les patients avec réarrangement d’ALK en première ligne) ou toxiques (toxicité potentielle des TKIs comme l’osimertinib prescrits de façon séquentielle à un traitement par immunothérapie qui aurait été initié sans attendre le statut moléculaire). Les principales altérations sont des mutations (mutations ponctuelles, insertions, délétions) et des fusions (réarrangements d’une portion de chromosome mettant « en contact » deux gènes initialement séparés et responsables de la formation d’une protéine dite de fusion). De façon générale, les mutations sont détectables par des techniques de séquençage sur l’ADN (NGS ADN) et sur l’ARN (RNAseq ou NGS ARN). Les fusions sont, quant à elles, plus difficiles à déterminer sur l’ADN, même si certains panels et techniques le permettent. Elles sont cependant retrouvées de façon plus classique en RNAseq. Petite particularité : les skipping de l’exon 14 de MET correspondent sur l’ADN à des mutations ponctuelles sur les sites d’épissage des introns et sont ainsi responsables, sur l’ARN, d’un saut complet de l’exon 14. Les exons 13 et 15 sont alors mis en contact, on peut aussi parler de fusion de l’exon 13 et 15 de MET. Ces mutations sur les sites d’épissage peuvent être détectées sur l’ADN, même si cela peut-être difficile, mais le saut de l’exon 14 est plus facilement détectable sur l’ARN. Dans ce tableau sont résumés les différents traitements disposant d’accès en France ou d’Autorisation de Mise sur le Marché (AMM) au moment de la rédaction de ce document. Plusieurs molécules disposent d’une AMM mais pas de remboursement en France dont les inhibiteurs de MET (tepotinib, capmatinib), de RET (pralsetinib, selpercatinib) et de NTRK (entrectinib, larotrectinib). Pour les mutations d’HER2 et les fusions de NRG1, des inhibiteurs spécifiques sont disponibles dans le cadre d’essais thérapeutiques uniquement. Quelle que soit l’altération, de nombreux essais évaluant de nouvelles molécules, des inhibiteurs de nouvelle génération ou de nouvelles stratégies sont ouverts sur le territoire et doivent être privilégiés quand cela est possible.