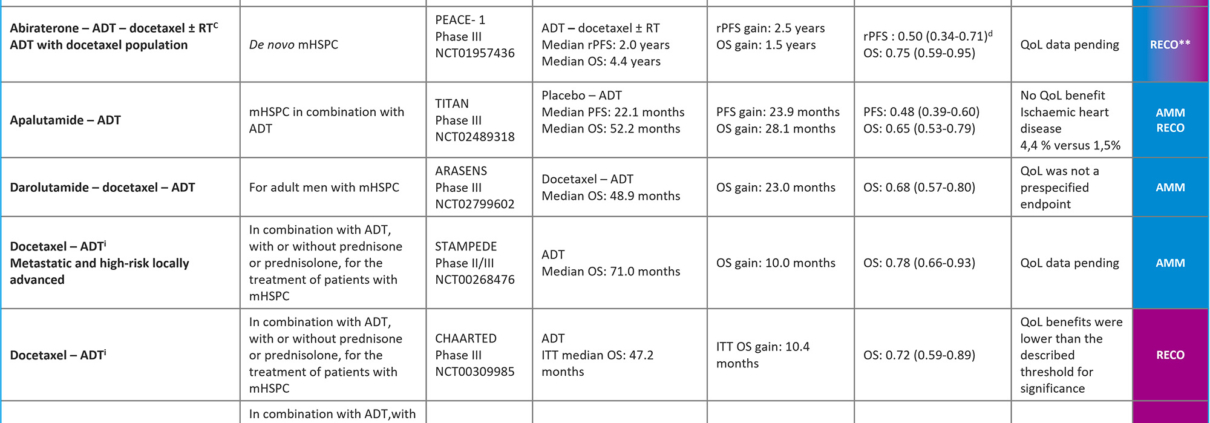
Escalade thérapeutique dans le traitement du mHSPC : quel agent pour quelle maladie ?
La prise en charge du cancer de la prostate métastatique hormonosensible bénéficie depuis désormais quelques années de l’arrivée des hormonothérapies dites de seconde génération (NHT). La première à avoir démontré son rôle a été l’acétate d’abiratérone, dans le cadre des essais LATITUDE puis STAMPEDE (Fizazi et al. Lancet Oncol 2019.20 :686-700 ; James et al. New Engl J Med 2017 ;377 :338-351). Successivement et rapidement, les anti-androgènes de seconde génération, apalutamide, darolutamide et enzalutamide ont également confirmé leur efficacité (Chi KN et al., J ClinOncol 2021.39 :2294-2303 ; Armstrong AJ et al. J Clin Oncol 2022.40 :1616-22 ; Davis ID et al. New Engl J Med 2019.381 :121-131). Si l’ajout de ces agents thérapeutiques à la déprivation androgénique s’est chaque fois traduit par un bénéfice tant en termes de survie sans progression radiologique, qu’en termes de survie globale, des différences concernant la présentation de la maladie, sur le plan chronologique synchrone/ de novo vs métachrone, ou sur le plan clinique haut volume, haut risque, s’observent selon le type de population sélectionnée pour les essais de phase III respectifs. Le tableau ci-dessus reprend les critères principaux des essais, leur design, et résultats en tant qu’objectifs primaires, les données de qualité de vie lorsque celles-ci sont disponibles, ou en attente. (ESMO guidelines e-update 2023) Dans le même temps, les recommandations CCAFU ont récemment précisé les critères de sélection des combinaisons (Ploussard et al. Prog Urol. 2022. 32:1372-1419). Ainsi, le doublet déprivation androgénique – NHT s’impose désormais à l’ensemble des patients, quel que soit le volume de la maladie métastatique, quel que soit le moment, synchrone ou après traitement local initial de la prostate, sous réserve de l’absence de contre-indication formelle et de l’éligibilité du patient tenant compte de ses comorbidités, voir après conciliation médicamenteuse si besoin et possible. Le choix de l’agent suivra les recommandations, AMM et remboursement. En contrepartie, la radiothérapie de la prostate ne sera proposée que chez les patients par définition avec une maladie synchrone et un faible volume métastatique (3 localisations secondaires osseuses maximum, localisations ganglionnaires et absence de localisation viscérale) (Ali A et al. JAMA Oncol 2021. 7 :555-563). La chimiothérapie par docetaxel, quant à elle, a trouvé sa place dans un premier temps dans le traitement des patients de haut volume métastatique. Désormais, ce sont les triplets qui sont à considérer, sur la base des données des essais, PEACE1 et ARASENS, chez les patients éligibles, synchrones et de haut volume (Fizazi K et al. Lancet 2022 ; Smith et al. NEJM 2022). La place du triplet chez les patients métachrones, ou de faible volume reste à préciser, et non recommandée en l’absence de données complémentaires (Ploussard, Prog Urol 2022).